¿Qué es la tabla periódica y por qué es tan importante en la química?
La tabla periódica es un recurso fundamental en el estudio de la química. Esta tabla organiza los elementos químicos de acuerdo a sus propiedades y características, proporcionando una estructura ordenada y comprensible para los científicos y estudiantes. Fue creada por el químico ruso Dmitri Mendeléyev en 1869 y desde entonces ha sido una herramienta esencial en el campo de la química.
La tabla periódica contiene información valiosa sobre cada uno de los elementos químicos conocidos. Cada elemento se representa por su símbolo único, como el «H» para el hidrógeno o el «O» para el oxígeno. Además, se clasifican en filas llamadas periodos y columnas llamadas grupos. Estas filas y columnas revelan patrones y tendencias en las propiedades químicas de los elementos, lo que permite hacer predicciones sobre su comportamiento y reactividad.
La estructura de la tabla periódica y su importancia en la química
La tabla periódica se divide en bloques, grupos y periodos. Comenzando desde la izquierda, el lado más largo contiene los metales, conocidos por su brillo, conductividad eléctrica y tendencia a ceder electrones. A medida que avanzamos hacia la derecha, encontramos los no metales, que son malos conductores de electricidad y tienden a ganar electrones. En el centro, tenemos los metaloides, que exhiben propiedades tanto de los metales como de los no metales.
Los periodos de la tabla periódica representan las capas de electrones que rodean el núcleo de un átomo. A medida que avanzamos de arriba abajo en la tabla, los periodos se van llenando con electrones adicionales, lo que aumenta la cantidad de energía en un átomo. Esto se debe a que cada periodo tiene una capa de electrones adicional en comparación con el periodo anterior.
Los grupos, por otro lado, representan las columnas verticales en la tabla periódica. Cada grupo comparte características similares debido a la configuración electrónica de los elementos. Por ejemplo, el grupo 1, también conocido como los metales alcalinos, son extremadamente reactivos y tienden a perder fácilmente un electrón para formar una carga positiva.
Propiedades periódicas y su relación con la tabla periódica
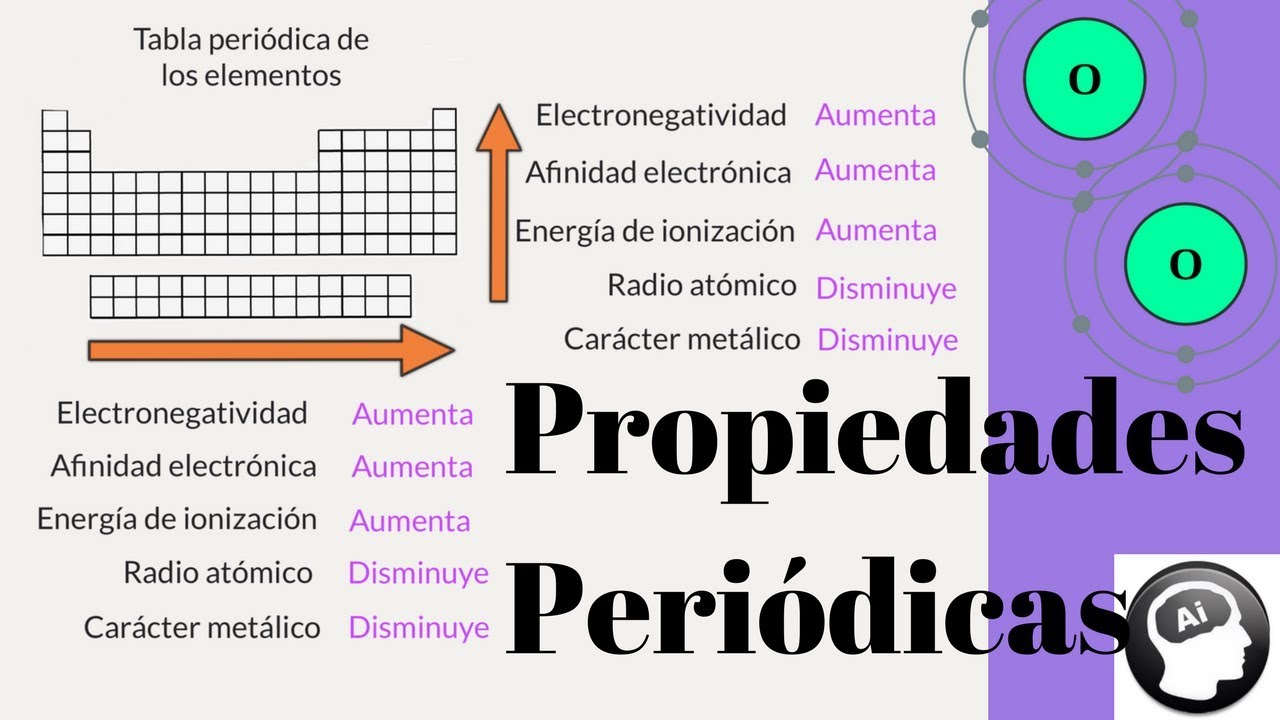
Las propiedades periódicas son características que se repiten en patrones a medida que avanzamos a través de la tabla periódica. Estas propiedades incluyen el tamaño atómico, la reactividad, la electronegatividad, la energía de ionización y la afinidad electrónica.
El tamaño atómico, por ejemplo, disminuye a medida que nos movemos de izquierda a derecha en un período, ya que hay una mayor atracción nuclear que comprime los electrones más cercanos al núcleo. Sin embargo, el tamaño atómico aumenta a medida que descendemos por un grupo, ya que se agrega una capa de electrones a la nube electrónica del átomo.
La reactividad también muestra patrones periódicos. Por ejemplo, los metales alcalinos en el grupo 1 son extremadamente reactivos y tienden a perder un electrón para formar iones positivos. Por otro lado, los halógenos en el grupo 17 son altamente reactivos y tienden a ganar un electrón para formar iones negativos.
Aplicaciones y utilidades de la tabla periódica
La tabla periódica es una herramienta esencial en el campo de la química y tiene una amplia variedad de aplicaciones y utilidades. Los científicos e ingenieros la utilizan para predecir las propiedades y comportamientos de los elementos y compuestos químicos en diversas situaciones.
En la industria, la tabla periódica es utilizada para desarrollar nuevos materiales y compuestos químicos con propiedades específicas. Por ejemplo, al comprender las propiedades de los diferentes elementos, los científicos pueden diseñar aleaciones de metales más resistentes o materiales superconductores para aplicaciones en la electrónica.
Además, la tabla periódica es una herramienta importante en la educación. Los estudiantes de química la utilizan para aprender y memorizar los elementos y sus propiedades, así como para comprender las relaciones entre ellos. También es útil para la resolución de problemas y ejercicios prácticos en el salón de clases.
¿Cuál es el elemento más abundante en la Tierra?
El elemento más abundante en la Tierra es el oxígeno, que constituye aproximadamente el 46% de la corteza terrestre y el 88% de la masa del agua.
¿Cuántos elementos químicos existen en la tabla periódica?
Actualmente, la tabla periódica contiene 118 elementos químicos conocidos. Sin embargo, se continúa investigando y descubriendo nuevos elementos en laboratorios de todo el mundo.
¿Cuál es el elemento más pesado de la tabla periódica?
El elemento más pesado de la tabla periódica es el oganesón (Og), con un número atómico de 118. Fue sintetizado por científicos rusos y estadounidenses en 2002.
¿Qué es la electronegatividad y cómo se relaciona con la tabla periódica?
La electronegatividad es una medida de la capacidad de un átomo para atraer electrones hacia sí mismo en un enlace químico. A medida que nos desplazamos de izquierda a derecha en la tabla periódica, la electronegatividad tiende a aumentar, ya que los átomos tienen una mayor capacidad para atraer electrones debido a una mayor carga nuclear.
¿Qué es la afinidad electrónica y cómo se relaciona con la tabla periódica?
La afinidad electrónica es la energía liberada cuando un átomo gana un electrón para formar un ion negativo. A medida que nos desplazamos de izquierda a derecha en la tabla periódica, la afinidad electrónica tiende a aumentar, ya que los átomos tienen una mayor tendencia a ganar electrones debido a una mayor carga nuclear y una menor distancia entre el núcleo y la capa electrónica externa.