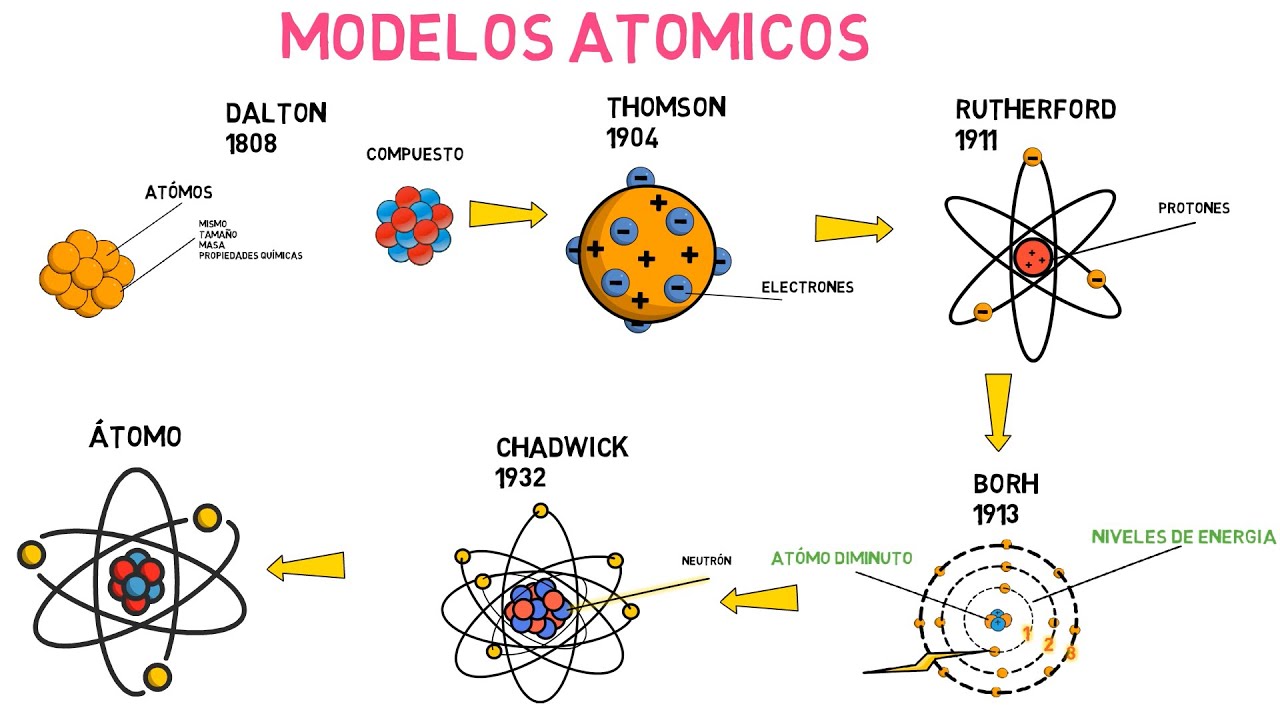
La estructura atómica antes del siglo XIX
En el pasado, la estructura atómica era un tema enigmático y desconocido para la humanidad. Durante siglos, los científicos se preguntaron cómo estaba compuesto el mundo material que nos rodea. Fue en el siglo XIX cuando comenzaron a surgir los primeros avances en nuestra comprensión de la estructura atómica. A continuación, exploraremos los hitos más importantes en la evolución de nuestra comprensión de los átomos.
La teoría atómica de Dalton (1803)
Uno de los primeros científicos en proponer una teoría sobre la estructura atómica fue John Dalton, un químico y físico inglés. En 1803, Dalton propuso que los átomos eran las unidades fundamentales de la materia y que cada elemento estaba compuesto por átomos idénticos en términos de tamaño, masa y propiedades. Esta teoría se convirtió en la base de la química moderna y sentó las bases para futuros descubrimientos.
La teoría de J.J. Thomson y el descubrimiento del electrón (1897)
A finales del siglo XIX, J.J. Thomson, un físico británico, realizó una serie de experimentos que revolucionaron nuestra comprensión de la estructura atómica. Utilizando un tubo de rayos catódicos, Thomson descubrió la existencia de una partícula subatómica conocida como el electrón. Este descubrimiento demostró que los átomos no eran indivisibles, como se creía anteriormente, y que contenían partículas cargadas negativamente.
El modelo atómico de Rutherford (1911)
En 1911, el físico Ernest Rutherford llevó a cabo el famoso experimento de la lámina de oro, que permitió establecer el modelo atómico más aceptado en ese momento. Rutherford dirigió partículas alfa a una lámina de oro y observó que algunas de ellas se desviaban o rebotaban, lo que indicaba la presencia de un núcleo central cargado positivamente. Este descubrimiento condujo a la idea de que los átomos tenían un núcleo denso en su centro y que la mayor parte del espacio estaba vacío.
El modelo atómico de Bohr (1913)
Poco después del experimento de Rutherford, el físico danés Niels Bohr propuso un nuevo modelo atómico que tuvo en cuenta el comportamiento de los electrones. Según el modelo de Bohr, los electrones se desplazan en órbitas alrededor del núcleo en niveles de energía específicos. Este modelo explicó correctamente las líneas espectrales observadas en los espectros atómicos y estableció las bases para futuros desarrollos en la comprensión de la estructura atómica.
…
¿Cuáles son las partículas subatómicas más importantes?
Las partículas subatómicas más importantes son el electrón, el protón y el neutrón.
¿Cómo influyeron los descubrimientos sobre la estructura atómica en la tecnología actual?
Los descubrimientos sobre la estructura atómica sentaron las bases para numerosas tecnologías, como la energía nuclear, la electrónica y la nanotecnología, que han tenido un impacto significativo en nuestra sociedad actual.
¿Se han realizado más descubrimientos sobre la estructura atómica desde el siglo XX?
Sí, desde los avances del siglo XX, se han realizado numerosos descubrimientos en el campo de la estructura atómica, como la existencia de partículas subatómicas aún más pequeñas, como los quarks y los leptones.
¿Cuál es la importancia de comprender la estructura atómica?
La comprensión de la estructura atómica es fundamental para nuestra comprensión de la química, la física y otras ramas de la ciencia. Además, ha abierto las puertas a numerosas tecnologías y aplicaciones prácticas que han transformado nuestra sociedad.