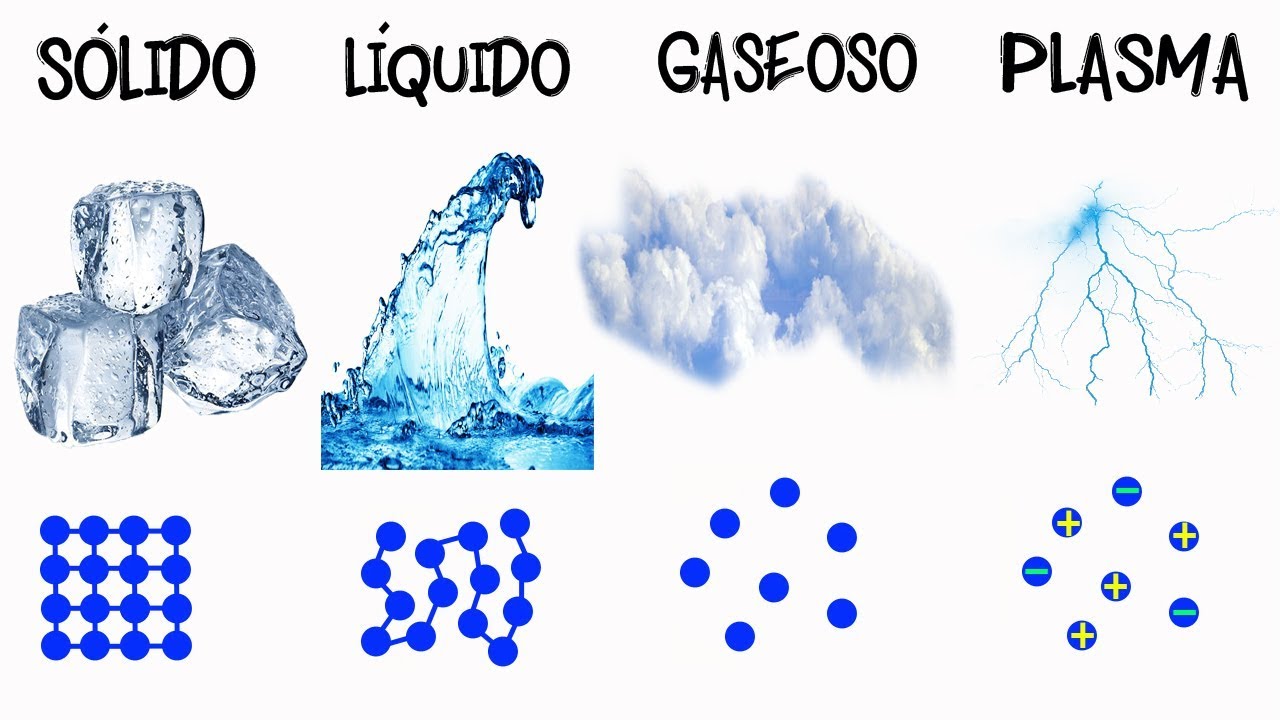
¿Qué son los estados de agregación de la materia?
En el estudio de la materia, una de las clasificaciones más importantes es la de los estados de agregación. Estos estados se refieren a las distintas formas en que la materia puede presentarse, dependiendo de las condiciones de temperatura y presión a las que se encuentra sometida. En total, existen cuatro estados de agregación conocidos: sólido, líquido, gaseoso y plasma. Cada uno de ellos tiene características y propiedades muy particulares que los diferencian entre sí. A continuación, te ofrecemos un completo esquema para que puedas comprender mejor cada uno de estos estados y su comportamiento.
Estado sólido: la estabilidad en las estructuras
El estado sólido es aquel en el que las partículas de una sustancia se encuentran muy cercanas entre sí, manteniendo una estructura rígida y compacta. En este estado, las partículas tienen una baja energía cinética, lo que significa que se encuentran en movimiento lento y apenas se desplazan de sus posiciones de equilibrio. Por esta razón, los sólidos tienen una forma y un volumen definidos.
Un ejemplo común de un sólido es el hielo. Cuando el agua se enfría por debajo de los 0°C, las moléculas de agua se organizan en una estructura ordenada, formando cristales de hielo. Esta estructura le da al hielo su forma y volumen característicos. Además, los sólidos son generalmente muy resistentes a los cambios de forma y compresión, lo que los hace ideales para construir estructuras estables y duraderas.
Continuando con el esquema de los estados de agregación, pasamos al estado líquido.
Estado líquido: fluidez y adaptabilidad
Cuando la materia se encuentra en estado líquido, las partículas se mantienen en contacto unas con otras, pero con mayor libertad de movimiento en comparación con los sólidos. Esto implica que los líquidos no tienen una forma definida, sino que adoptan la forma del recipiente que los contiene. Sin embargo, los líquidos sí tienen un volumen definido.
Un ejemplo claro de líquido es el agua. A temperatura ambiente, las moléculas de agua se mueven constantemente, deslizándose unas sobre otras. Este movimiento hace que el agua sea fluida y capaz de adaptarse a diferentes recipientes. Además, los líquidos son fácilmente compresibles y presentan una mayor viscosidad en comparación con los gases.
Continuando con nuestro esquema de los estados de agregación, llegamos al estado gaseoso.
Estado gaseoso: libertad absoluta
Cuando una sustancia se encuentra en estado gaseoso, sus partículas se encuentran muy separadas entre sí y se mueven de manera desordenada, con una alta energía cinética. Esto significa que los gases no tienen una forma ni un volumen definidos, ya que se expanden para llenar completamente el espacio que se les proporciona.
Ejemplos comunes de gases son el oxígeno y el dióxido de carbono. Estas sustancias se presentan en forma gaseosa debido a las condiciones de temperatura y presión en las que se encuentran. Los gases son altamente compresibles y suelen tener una baja viscosidad, lo que les permite difundirse rápidamente en el aire y llenar cualquier espacio disponible.
Por último, pero no menos importante, en nuestro completo esquema de los estados de agregación, abordamos el estado de plasma.
Estado de plasma: energía y luminosidad
El estado de plasma es menos común en la Tierra, pero se encuentra ampliamente presente en el universo. En este estado, las partículas se ionizan, es decir, pierden o ganan electrones, generando así una gran cantidad de iones positivos y negativos. Como resultado, el plasma se caracteriza por su alta conductividad eléctrica y su capacidad de emitir luz.
Un excelente ejemplo de plasma es el sol. En su núcleo, el sol alcanza temperaturas extremadamente altas, lo que hace que los átomos se ionizen y se conviertan en un plasma luminoso. Además del sol, los rayos durante una tormenta también se consideran plasma debido a la gran concentración de iones presentes.
En resumen, los estados de agregación de la materia son fundamentales para comprender y explicar la forma en que la materia se presenta en diferentes condiciones ambientales. Desde la rigidez y estabilidad de los sólidos hasta la adaptabilidad y fluidez de los líquidos, pasando por la libertad y expansión de los gases, y llegando a la energía y luminosidad del plasma, cada estado tiene sus propias características y comportamientos únicos.