Descubre los distintos sistemas termodinámicos
La termodinámica es una rama de la física que estudia las propiedades de la energía y las relaciones entre el calor y el trabajo. Una de las principales clasificaciones en termodinámica es la de los sistemas termodinámicos. Estos sistemas son una parte fundamental de la termodinámica, ya que nos permiten analizar y entender cómo se comporta la energía en diferentes entornos.
¿Qué es un sistema termodinámico?
Un sistema termodinámico se define como una parte del universo que se encuentra bajo estudio o análisis. Puede ser cualquier objeto o conjunto de objetos que se aísle del entorno para poder analizar sus propiedades y su interacción con la energía. El estudio de los sistemas termodinámicos es crucial para entender cómo funciona la energía en diversos procesos físicos.
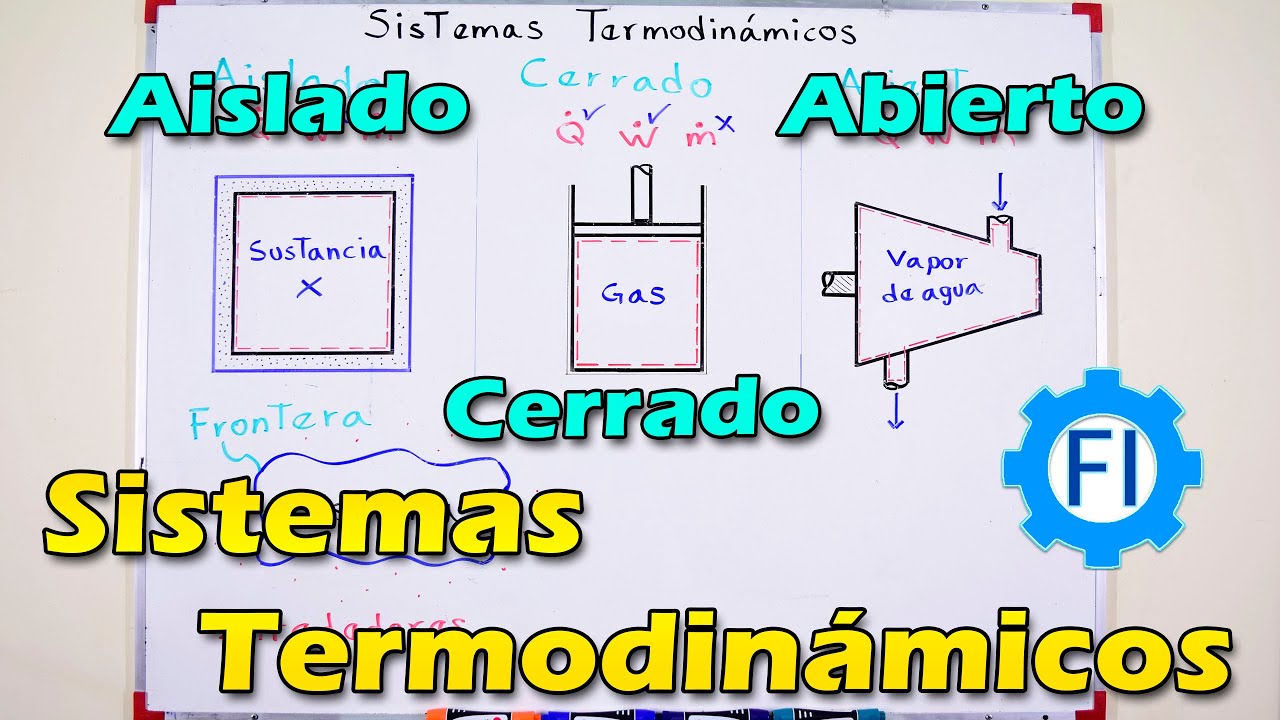
Existen diferentes tipos de sistemas termodinámicos y cada uno de ellos se clasifica según su interacción con su entorno. A continuación, te presentamos los cuatro tipos principales:
Sistema cerrado: Es aquel que no intercambia materia con su entorno, pero sí intercambia energía en forma de calor o trabajo. Por ejemplo, un recipiente de agua cerrado que se calienta o se enfría.
Sistema abierto: En contraste con el sistema cerrado, este tipo de sistema sí permite el intercambio de materia y energía con su entorno. Podemos considerar un río como un ejemplo de sistema abierto, ya que permite la entrada y salida de agua.
Sistema aislado: Un sistema aislado no permite el intercambio de energía ni con su entorno ni con otros sistemas. Es decir, no hay transferencia de calor ni trabajo. Un ejemplo de esto puede ser un termo completamente sellado y sin pérdidas de calor.
Sistema adiabático: Este tipo de sistema no permite el intercambio de calor con su entorno, pero sí permite el intercambio de energía en forma de trabajo. Puedes pensar en una caja herméticamente cerrada que realiza trabajo mecánico sin intercambio de calor.
Ahora que conoces las clasificaciones básicas de los sistemas termodinámicos, es importante comprender cómo se relacionan con los principios fundamentales de la termodinámica. Estos principios, conocidos como las leyes de la termodinámica, establecen las reglas que rigen el comportamiento de la energía en los sistemas.
La primera ley de la termodinámica, también conocida como el principio de conservación de la energía, establece que la energía total de un sistema aislado se mantiene constante. Esto significa que la energía no puede ser creada ni destruida, solo transferida o transformada entre diferentes formas.
La segunda ley de la termodinámica, a su vez, establece que la entropía de un sistema aislado siempre tiende a aumentar. La entropía se define como el grado de desorden o degradación de la energía en un sistema. Esta ley nos lleva a comprender por qué el calor siempre fluye de áreas de alta temperatura a áreas de baja temperatura y por qué los procesos naturales tienden a aumentar la entropía del universo.
Es importante destacar que estos principios se aplican a todos los sistemas termodinámicos, sin importar su clasificación. Desde un simple vaso de agua caliente hasta un complejo motor de combustión interna, las leyes de la termodinámica son fundamentales para comprender cómo se comporta la energía en cada uno de ellos.
Los sistemas termodinámicos son una parte fundamental en el estudio de la termodinámica y nos permiten entender cómo se comporta la energía en diferentes entornos. La clasificación de los sistemas termodinámicos según su interacción con su entorno es clave para analizar y comprender su comportamiento. Ya sea un sistema cerrado, abierto, aislado o adiabático, cada uno tiene características y propiedades únicas que rigen el intercambio de energía.
La termodinámica y los sistemas termodinámicos son fundamentales en muchos campos científicos y tecnológicos, como la ingeniería, la física y la química. Comprender los principios y clasificaciones de los sistemas termodinámicos nos permite resolver problemas y diseñar procesos más eficientes que aprovechen la energía de forma más efectiva.
1. ¿Cuál es la diferencia entre un sistema abierto y un sistema cerrado?
En un sistema abierto, se permite el intercambio de materia y energía con su entorno, mientras que en un sistema cerrado solo se permite el intercambio de energía.
2. ¿Cuál es la importancia de la clasificación de sistemas termodinámicos?
La clasificación de sistemas termodinámicos nos ayuda a entender y analizar cómo la energía interactúa con diferentes entornos, lo que es crucial para resolver problemas y diseñar procesos eficientes.
3. ¿Cómo se relacionan los sistemas termodinámicos con las leyes de la termodinámica?
Los sistemas termodinámicos son el objeto de estudio de las leyes de la termodinámica. Estas leyes establecen los principios fundamentales que rigen el comportamiento de la energía en los sistemas.
4. ¿Qué es la entropía y por qué es importante en la termodinámica?
La entropía es una medida del desorden o degradación de la energía en un sistema. Es importante en termodinámica porque la segunda ley establece que la entropía de un sistema aislado siempre tiende a aumentar.
5. ¿Cuáles son algunos ejemplos de sistemas adiabáticos?
Un ejemplo de sistema adiabático puede ser una caja herméticamente cerrada que realiza trabajo mecánico sin intercambio de calor. También se puede considerar un gas contenido en un cilindro con paredes aislantes térmicamente como un sistema adiabático.