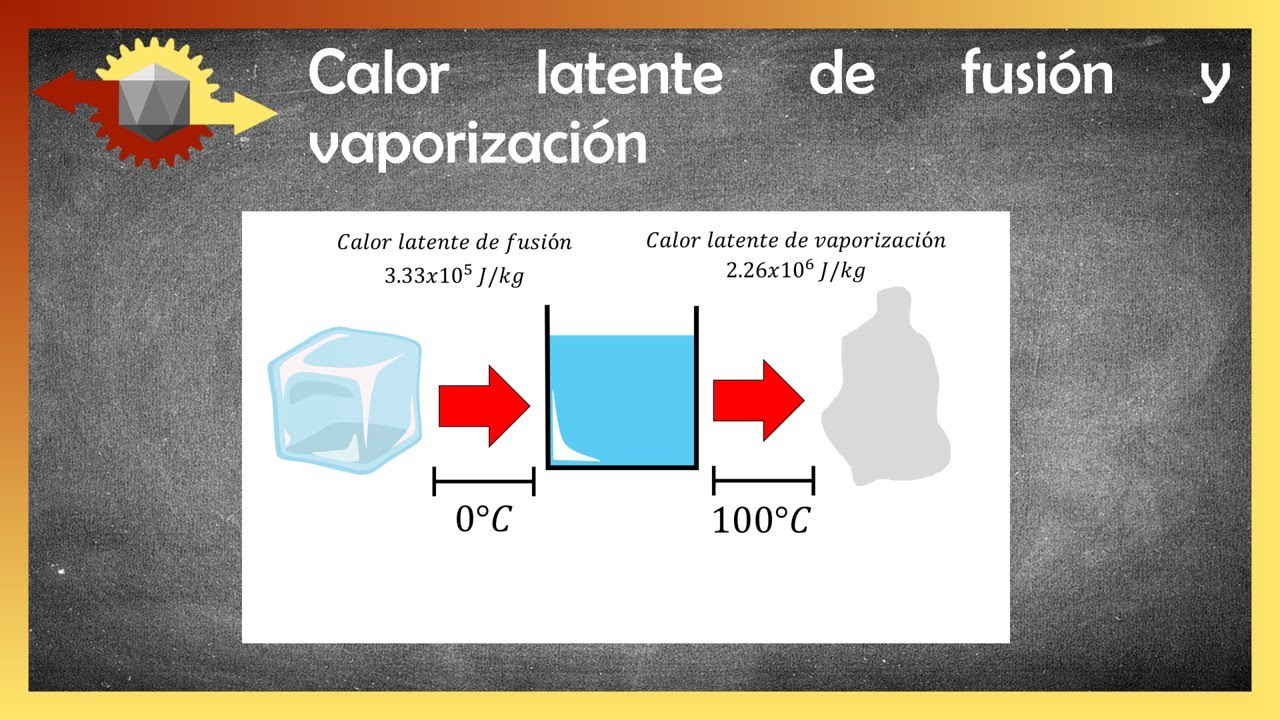
El calor latente es una propiedad física de la materia que se refiere a la cantidad de energía térmica necesaria para que ocurra un cambio de fase a temperatura constante. En este artículo, exploraremos los conceptos de calor latente de fusión, vaporización y sublimación, y entenderemos cómo estas transiciones de fase ocurren en distintas sustancias.
¿Qué es el calor latente de fusión?
Cuando una sustancia pasa de su estado sólido a su estado líquido, se requiere una cantidad de energía térmica específica para romper las fuerzas de atracción entre las moléculas y permitir que estas se muevan con mayor libertad. A esta cantidad de energía se le conoce como calor latente de fusión.
Cada sustancia tiene un valor único de calor latente de fusión, el cual se expresa en unidades de energía por masa, como julios por gramo (J/g) o calorías por gramo (cal/g). Este valor representa la cantidad de energía necesaria para fundir un gramo de la sustancia a su temperatura de fusión. Por ejemplo, el agua tiene un calor latente de fusión de aproximadamente 334 J/g.
¿Cómo se calcula el calor latente de fusión?
El calor latente de fusión se calcula utilizando la fórmula:
Q = m * L
Donde Q es la cantidad de calor latente de fusión en julios, m es la masa de la sustancia en gramos y L es el valor del calor latente de fusión en J/g.
Por ejemplo, si tenemos 10 gramos de agua y queremos calcular la cantidad de calor necesaria para fundirla, utilizando el valor del calor latente de fusión del agua de 334 J/g, podemos calcularlo de la siguiente manera:
Q = 10 g * 334 J/g = 3340 J
¿Qué es el calor latente de vaporización?
Cuando una sustancia pasa de su estado líquido a su estado gaseoso, se requiere una cantidad adicional de energía térmica para romper completamente las fuerzas intermoleculares y permitir que las moléculas se conviertan en gas. A esta cantidad de energía se le conoce como calor latente de vaporización.
Al igual que el calor latente de fusión, el calor latente de vaporización es una propiedad específica de cada sustancia y se expresa en unidades de energía por masa, como julios por gramo (J/g) o calorías por gramo (cal/g).
¿Cómo se calcula el calor latente de vaporización?
El calor latente de vaporización también se calcula utilizando la fórmula:
Q = m * L
Donde Q es la cantidad de calor latente de vaporización en julios, m es la masa de la sustancia en gramos y L es el valor del calor latente de vaporización en J/g.
Por ejemplo, si tenemos 10 gramos de agua líquida y queremos calcular la cantidad de calor necesaria para convertirla en vapor, utilizando el valor del calor latente de vaporización del agua de aproximadamente 2260 J/g, podemos calcularlo de la siguiente manera:
Q = 10 g * 2260 J/g = 22600 J
¿Qué es el calor latente de sublimación?
El calor latente de sublimación se refiere a la cantidad de energía térmica necesaria para que una sustancia pase directamente de su estado sólido a su estado gaseoso, sin pasar por el estado líquido intermedio. Como en los casos anteriores, el calor latente de sublimación es una propiedad específica de cada sustancia y se expresa en unidades de energía por masa.
Un ejemplo común de sublimación es el hielo seco, que es dióxido de carbono en estado sólido. Cuando el hielo seco se expone al aire, sublima directamente en gas sin pasar por el estado líquido.
¿Cómo se calcula el calor latente de sublimación?
El calor latente de sublimación también se calcula utilizando la fórmula:
Q = m * L
Donde Q es la cantidad de calor latente de sublimación en julios, m es la masa de la sustancia en gramos y L es el valor del calor latente de sublimación en J/g.
Por ejemplo, si tenemos 10 gramos de hielo seco y queremos calcular la cantidad de calor necesaria para que se sublime, utilizando el valor del calor latente de sublimación del dióxido de carbono de aproximadamente 571 J/g, podemos calcularlo de la siguiente manera:
Q = 10 g * 571 J/g = 5710 J
El calor latente de fusión, vaporización y sublimación son conceptos fundamentales en la física de las transiciones de fase. Estas propiedades nos permiten entender cómo las sustancias cambian de estado y cómo se requiere una cantidad específica de energía térmica para que esto ocurra.
Es importante destacar que el calor latente de fusión, vaporización y sublimación varía entre las diferentes sustancias y depende de factores como la temperatura y la presión. Estas propiedades juegan un papel crucial en fenómenos naturales como la formación de nubes, la solidificación de metales y la evaporación del agua.
Esperamos que este artículo te haya brindado una mejor comprensión del calor latente y su importancia en los cambios de fase. Si tienes alguna pregunta adicional o deseas profundizar en algún aspecto en particular, no dudes en dejarnos un comentario.