¿Qué es la configuración electrónica y por qué es importante?
La configuración electrónica de un elemento es la distribución de sus electrones en los diferentes niveles, subniveles y orbitales de un átomo. Es esencial comprender la configuración electrónica de los elementos porque determina sus propiedades químicas y su comportamiento en las reacciones químicas.
¿Cómo se determina la configuración electrónica de los elementos?
La configuración electrónica se determina siguiendo una serie de reglas y principios establecidos en la teoría cuántica. A continuación, te mostraré un método paso a paso para determinar la configuración electrónica de cualquier elemento.
Identifica el número atómico del elemento
El número atómico de un elemento, que se encuentra en la tabla periódica, es la cantidad de protones que tiene en su núcleo. Por ejemplo, el número atómico del hidrógeno es 1, el del helio es 2, y así sucesivamente.
Distribuye los electrones en los niveles
Los electrones se distribuyen en diferentes niveles energéticos alrededor del núcleo. El primer nivel puede contener hasta 2 electrones, el segundo hasta 8 electrones, el tercero hasta 18 electrones y así sucesivamente.
Llena los orbitales dentro de cada nivel
Cada nivel se divide en subniveles y orbitales. Los subniveles se representan con letras (s, p, d, f) y los orbitales con números (0, 1, 2, 3). Cada orbital puede contener una cantidad específica de electrones.
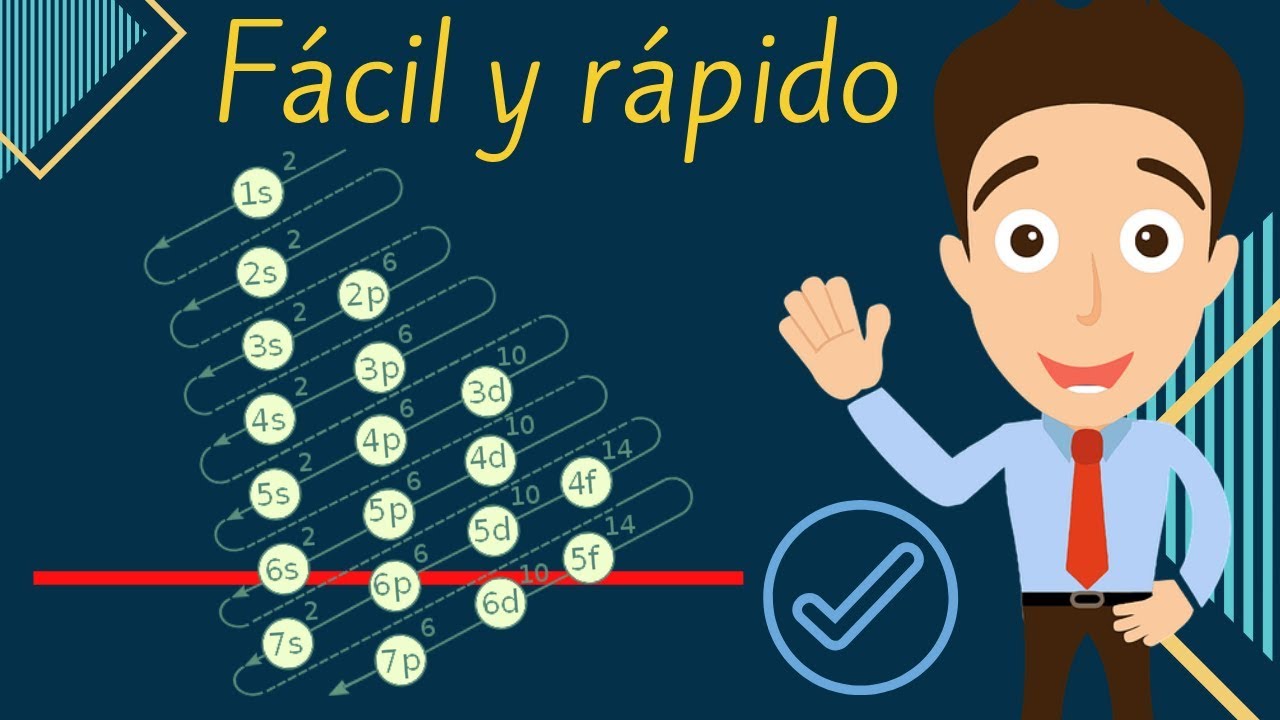
Sigue la regla de Aufbau
La regla de Aufbau establece que los electrones llenan los orbitales en orden ascendente de energía. Es decir, se llenan primero los orbitales de menor energía antes de pasar a los de mayor energía.
Continúa siguiendo estos pasos para completar la configuración electrónica del elemento que estés analizando. Recuerda que debes tener en cuenta las excepciones y las configuraciones electrónicas especiales de algunos elementos.
Aplicaciones de la configuración electrónica
La configuración electrónica de los elementos tiene muchas aplicaciones en la química y otras disciplinas científicas. Algunas de las aplicaciones son:
Predicción de las propiedades químicas
La configuración electrónica determina cómo reaccionará un elemento con otros elementos. Por ejemplo, los elementos con configuraciones electrónicas similares tienden a tener propiedades químicas similares.
Explicación de la conductividad eléctrica
La configuración electrónica influye en la capacidad de un material para conducir la electricidad. Los materiales con configuraciones electrónicas que les permiten tener electrones libres tienden a ser buenos conductores eléctricos.
Diseño de nuevos materiales
El conocimiento de la configuración electrónica permite a los científicos diseñar nuevos materiales con propiedades específicas. Pueden manipular la configuración electrónica para crear materiales más resistentes, más flexibles o con otras características deseables.
¿Qué es un orbital?
Un orbital es una región del espacio donde es probable que se encuentre un electrón. Cada orbital puede contener hasta dos electrones con espines opuestos.
¿Cuáles son las excepciones a la regla de Aufbau?
Algunos elementos tienen excepciones en su configuración electrónica debido a su tendencia a ser más estables al tener ciertas configuraciones. Por ejemplo, el cromo y el cobre tienen una configuración electrónica especial para lograr mayor estabilidad.
¿Cómo puedo recordar la configuración electrónica de todos los elementos?
Memorizar la configuración electrónica de todos los elementos puede ser abrumador. Sin embargo, puedes encontrar patrones y tendencias en la tabla periódica que te ayudarán a recordar las configuraciones electrónicas comunes. También puedes utilizar recursos en línea o aplicaciones que faciliten este proceso.
En conclusión, la configuración electrónica de los elementos es fundamental para comprender las propiedades y el comportamiento de los mismos. Al seguir algunos pasos y reglas establecidas, puedes determinar la configuración electrónica de cualquier elemento. Este conocimiento tiene diversas aplicaciones en la química y otras ciencias, y te permite entender mejor el mundo que te rodea.