La curva de titulación ácido fuerte-base débil es un concepto fundamental en la química analítica que nos permite entender cómo varía el pH de una solución a medida que se añade una base a un ácido fuerte. En este artículo, exploraremos en detalle esta curva de titulación, desde su definición hasta sus aplicaciones prácticas. Acompáñanos mientras te sumerges en este fascinante mundo de la química.
¿Qué es una curva de titulación?
Antes de adentrarnos en los detalles de la curva de titulación ácido fuerte-base débil, es importante comprender qué es una curva de titulación en general. Una curva de titulación es una representación gráfica de cómo varía una propiedad de una solución a medida que se añade de forma gradual un reactivo a dicha solución. En el caso de la curva de titulación ácido fuerte-base débil, la propiedad que varía es el pH de la solución.
Paso 1: Preparación de la solución
El primer paso para construir una curva de titulación ácido fuerte-base débil es preparar la solución inicial que se someterá a titulación. Para ello, necesitaremos un ácido fuerte, como el ácido clorhídrico (HCl), y una base débil, como el ácido acético (CH3COOH). Ambas sustancias se disolverán en agua para obtener las soluciones iniciales de ácido y base.
Paso 2: Medición del pH inicial
Una vez preparadas las soluciones iniciales, se medirá el pH de la solución ácida antes de comenzar la titulación. Para ello, se utilizará un medidor de pH o papel indicador, colocando una pequeña muestra de la solución en el electrodo o en el papel respectivamente. El pH inicial nos servirá como punto de partida para construir la curva de titulación.
Paso 3: Titulación
La titulación consiste en añadir de forma gradual la base débil a la solución ácida, mientras se va registrando el pH de la solución en cada punto de titulación. Esto se logra utilizando una bureta para agregar la base gota a gota, y un electrodo de pH para medir el pH de la solución.
1 Punto de equivalencia
Durante la titulación, llegará un momento en el que la cantidad de base añadida será suficiente para neutralizar completamente el ácido presente en la solución. Este punto se conoce como el punto de equivalencia, y en este punto el pH de la solución será neutro, alrededor de 7.
2 Zona de transición
Antes de alcanzar el punto de equivalencia, la adición de la base débil irá provocando cambios en el pH de la solución. Se observará una zona de transición, en la cual el pH comenzará a desviarse del valor inicial, indicando que la titulación está teniendo efecto. La forma y la ubicación de esta zona de transición dependerá de las particularidades de cada ácido y base utilizados.
Paso 4: Construcción de la curva de titulación
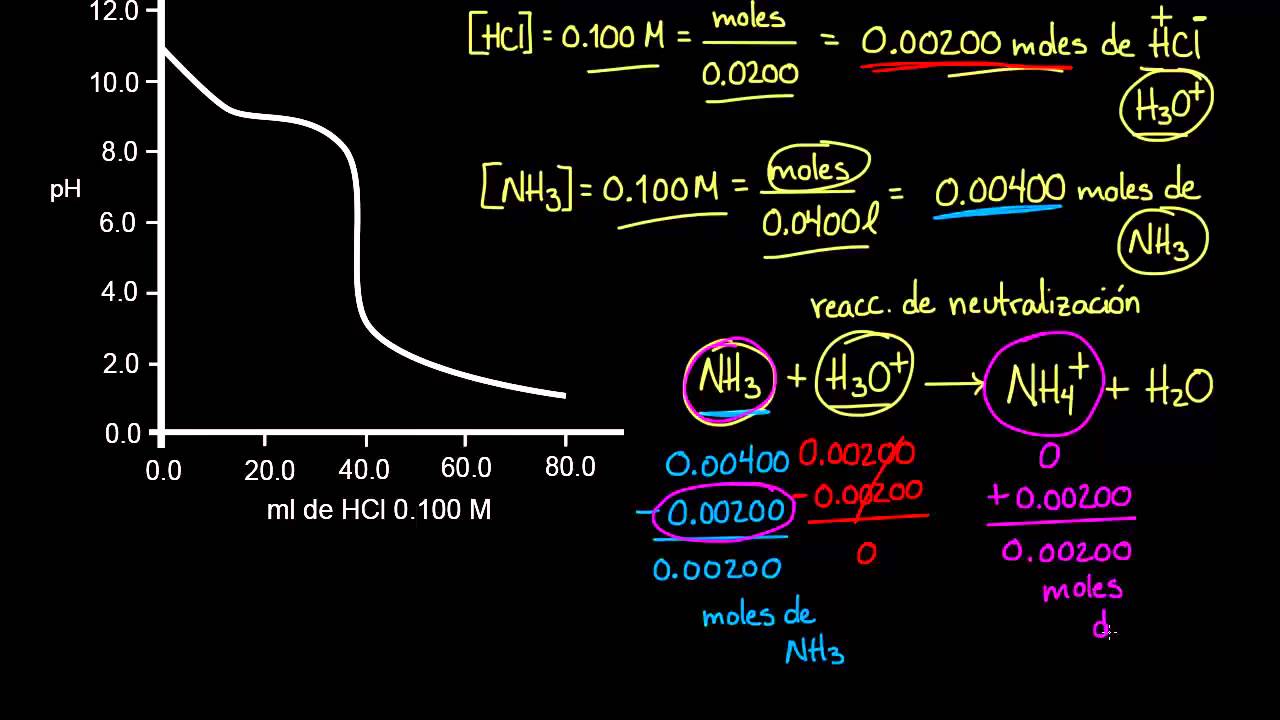
Una vez completada la titulación y registrados los valores de pH en cada punto, se pueden utilizar estos datos para construir la curva de titulación ácido fuerte-base débil. En esta curva, el eje x representa el volumen de base agregada, mientras que el eje y representa el pH de la solución.
1 Región ácida
Antes de la adición de la base débil, la solución se encuentra en la región ácida de la curva de titulación. En esta región, el pH será bajo, ya que la solución es ácida debido a la presencia del ácido fuerte.
2 Región de la zona de transición
Durante la adición de la base, se alcanzará la zona de transición, donde el pH comenzará a aumentar gradualmente. Esta región de la curva de titulación nos permite observar cómo el pH evoluciona a medida que se añade la base débil.
3 Región básica
Después de alcanzar el punto de equivalencia, la solución entra en la región básica de la curva de titulación, donde el pH se mantiene alto debido a la presencia de la base en exceso.
Aplicaciones prácticas de la curva de titulación
La curva de titulación ácido fuerte-base débil tiene numerosas aplicaciones en la química analítica. Algunas de ellas incluyen la determinación de la concentración de ácidos y bases en una muestra desconocida, la identificación de ácidos y bases desconocidos, y el cálculo del pH de una solución en función del volumen de base añadida.
¿Qué sucede si utilizo un ácido débil en lugar de un ácido fuerte en la titulación?
Utilizar un ácido débil en lugar de un ácido fuerte cambiará los resultados de la titulación, ya que el punto de equivalencia y la forma de la curva de titulación serán diferentes. La presencia de un ácido débil dará lugar a una curva de titulación más gradual y a un punto de equivalencia menos definido.
¿Qué ocurre si utilizo una base fuerte en lugar de una base débil en la titulación?
Al utilizar una base fuerte en lugar de una base débil, se esperará una curva de titulación diferente. La presencia de una base fuerte dará lugar a una curva de titulación más rápida, con una zona de transición más estrecha y un cambio de pH más pronunciado.
¿Es posible realizar una curva de titulación entre un ácido débil y una base débil?
Sí, es posible realizar una curva de titulación entre un ácido débil y una base débil. Sin embargo, este tipo de titulación es menos común y suele ser más complicado de interpretar debido a la falta de una diferencia de pH clara en el punto de equivalencia. Se requeriría un análisis más detallado de los resultados obtenidos.
¿Cuál es la importancia de la curva de titulación en el contexto de la química analítica?
La curva de titulación es una herramienta fundamental en la química analítica, ya que nos permite conocer información crucial sobre las características ácido-base de una sustancia. A través de la construcción de la curva de titulación, es posible determinar la concentración de ácidos y bases, identificar sustancias desconocidas y calcular el pH de una solución en función del volumen de reactivo añadido.