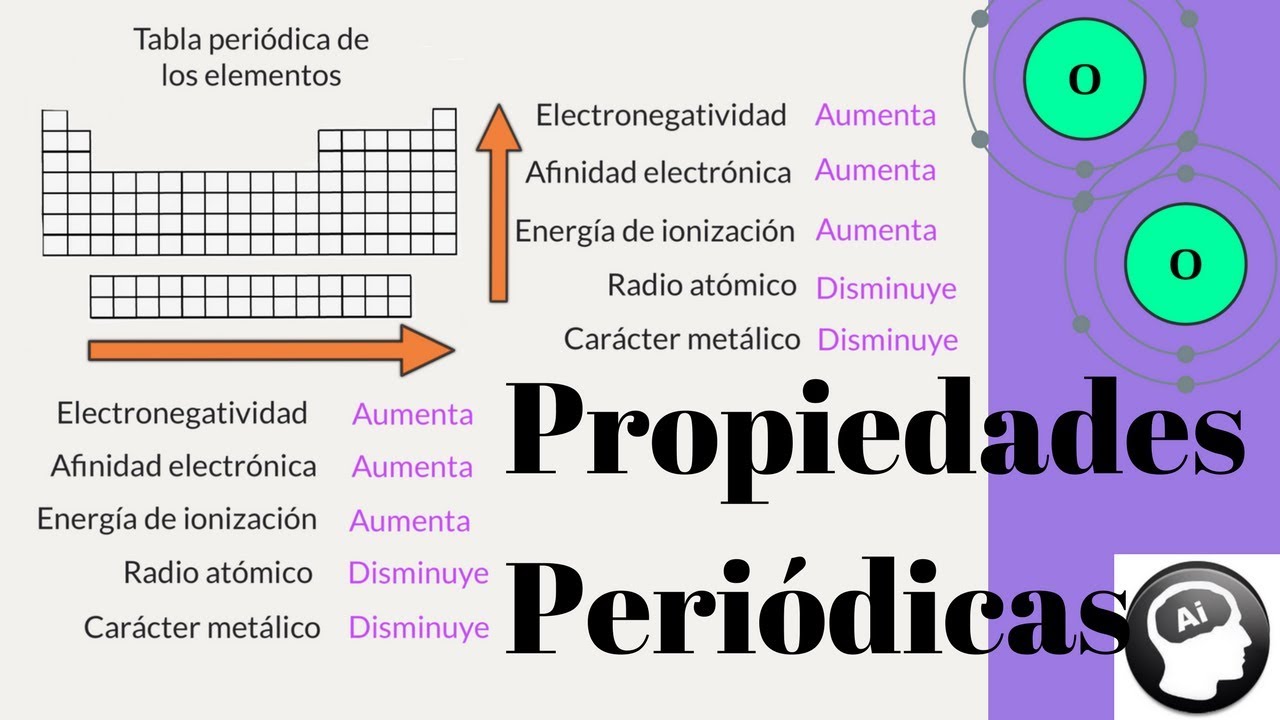
Encabezado: ¿Qué son las propiedades físicas de la tabla periódica?
La tabla periódica es una herramienta fundamental en el estudio de la química, ya que nos brinda información organizada sobre todos los elementos químicos conocidos. Además de proporcionarnos datos sobre su número atómico, masa atómica y configuración electrónica, la tabla periódica también nos permite comprender las propiedades físicas de estos elementos.
Punto de fusión y ebullición
Una de las propiedades físicas más básicas que se pueden obtener de la tabla periódica es el punto de fusión y ebullición de cada elemento. El punto de fusión es la temperatura a la cual una sustancia pasa de estado sólido a líquido, mientras que el punto de ebullición es la temperatura a la cual una sustancia pasa de estado líquido a gaseoso.
Al observar las diferentes filas de la tabla periódica, podemos notar que existe una tendencia general hacia el aumento del punto de fusión y ebullición a medida que avanzamos de izquierda a derecha y de abajo hacia arriba. Esto se debe a la estructura de los átomos y la fuerza de las atracciones intermoleculares presentes en cada elemento.
1 Factores que influyen en el punto de fusión y ebullición
Varios factores pueden influir en el punto de fusión y ebullición de un elemento. Entre ellos, se encuentran:
- Masa atómica: En general, cuanto mayor sea la masa atómica de un elemento, mayores serán sus puntos de fusión y ebullición.
- Tamaño del átomo: A medida que aumenta el tamaño del átomo, disminuyen las fuerzas de atracción entre los átomos, lo que puede resultar en puntos de fusión y ebullición más bajos.
- Número de electrones de valencia: Los elementos con una mayor cantidad de electrones de valencia tienden a tener puntos de fusión y ebullición más altos, debido a una mayor fuerza de atracción entre las moléculas.
- Configuración electrónica: La configuración electrónica de un elemento puede influir en las fuerzas de interacción entre las moléculas, lo que a su vez afecta sus puntos de fusión y ebullición.
Densidad
Otra propiedad física que se puede obtener de la tabla periódica es la densidad de los elementos. La densidad es la relación entre la masa y el volumen de una sustancia, y puede variar ampliamente entre los diferentes elementos.
Al analizar la tabla periódica, podemos observar que los elementos más pesados tienden a tener una mayor densidad que los elementos más ligeros. Esto se debe a que los átomos más pesados tienen una mayor masa y, por lo tanto, ocupan un volumen más pequeño en comparación con los átomos más ligeros.
1 Relación entre densidad y posición en la tabla periódica
Existen algunas tendencias generales en cuanto a la densidad de los elementos en la tabla periódica. Algunas de estas tendencias son:
- Metales: Los metales en general tienen una alta densidad. Esto se debe a la compactación de los átomos en la estructura metálica y a las fuerzas de atracción entre ellos.
- No metales: Los no metales tienden a tener densidades más bajas en comparación con los metales. Esto se debe a que los átomos de los no metales tienen una estructura más suelta y están menos densamente empaquetados.
- Transición: Los elementos de transición suelen tener densidades intermedias. Esto se debe a la variabilidad en las estructuras atómicas y a las diferentes fuerzas de atracción presentes en estos elementos.
Conductividad térmica y eléctrica
La tabla periódica también proporciona información sobre la conductividad térmica y eléctrica de los elementos. La conductividad térmica se refiere a la capacidad de un material para conducir el calor, mientras que la conductividad eléctrica se refiere a su capacidad para conducir la electricidad.
Los metales son conocidos por su alta conductividad tanto térmica como eléctrica. Esto se debe a la estructura metálica, que permite un fácil movimiento de los electrones en el material. Por otro lado, los no metales suelen tener una baja conductividad térmica y eléctrica, debido a su estructura molecular más compacta y a la falta de electrones móviles.
1 Excepciones a la regla
Si bien los metales y no metales siguen generalmente las tendencias en cuanto a la conductividad térmica y eléctrica, existen algunas excepciones en la tabla periódica. Algunos elementos, como el grafito, son considerados no metales pero tienen una alta conductividad eléctrica debido a su estructura de capas de grafeno.
Radio atómico
El radio atómico es una propiedad física importante que se puede obtener de la tabla periódica. Se refiere al tamaño de un átomo y se mide desde el centro del núcleo hasta la capa más externa de electrones.
Generalmente, a medida que avanzamos de izquierda a derecha en la tabla periódica, el radio atómico tiende a disminuir. Esto se debe a que los átomos se vuelven más pequeños y tienen más protones en el núcleo, lo que aumenta la fuerza de atracción entre el núcleo y los electrones.
1 Tendencia en el radio atómico
Al observar las filas y columnas de la tabla periódica, podemos notar algunas tendencias adicionales en cuanto al radio atómico:
- Radio atómico en los periodos: A medida que avanzamos en un período de la tabla periódica, el radio atómico generalmente disminuye. Esto se debe a la mayor carga nuclear efectiva, es decir, la atracción entre el núcleo y los electrones se vuelve más fuerte a medida que aumenta la carga nuclear.
- Radio atómico en los grupos: A medida que descendemos en un grupo de la tabla periódica, el radio atómico generalmente aumenta. Esto se debe a que los electrones ocupan capas de energía más externas, lo que aumenta la distancia promedio entre el núcleo y los electrones.
Electronegatividad
La electronegatividad es una propiedad física que nos indica la capacidad de un átomo para atraer electrones en un enlace químico. Esta propiedad puede influir en la forma en que los elementos interactúan entre sí y en las propiedades químicas resultantes.
En la tabla periódica, la electronegatividad suele aumentar a medida que avanzamos de izquierda a derecha y de abajo hacia arriba. Esto se debe a que los átomos más pequeños tienen una mayor atracción sobre los electrones en comparación con los átomos más grandes.
1 Importancia de la electronegatividad
La electronegatividad es una propiedad fundamental en la formación de enlaces químicos y determina la polaridad de las moléculas. Los elementos con una alta electronegatividad tienden a atraer electrones con mayor fuerza, lo que resulta en enlaces más polarizados.
Por ejemplo, en la molécula de agua (H2O), el oxígeno es más electronegativo que el hidrógeno, lo que resulta en un enlace polar donde el oxígeno tiene una ligera carga negativa y los hidrógenos tienen una ligera carga positiva.
La tabla periódica es una herramienta esencial para comprender las propiedades físicas de los elementos químicos. A través del análisis de esta tabla, podemos obtener información sobre el punto de fusión y ebullición, densidad, conductividad térmica y eléctrica, radio atómico y electronegatividad de cada elemento.
Estas propiedades físicas nos ayudan a entender cómo los átomos se comportan y cómo interactúan entre sí en las diversas reacciones químicas. Comprender las propiedades físicas de la tabla periódica es fundamental para el estudio de la química y tiene aplicaciones en campos como la ingeniería de materiales, la metalurgia y la investigación científica.
¿Qué es el punto de fusión en la tabla periódica?
El punto de fusión es la temperatura a la cual un elemento pasa de estado sólido a líquido. En la tabla periódica, podemos observar que existe una tendencia general hacia el aumento del punto de fusión a medida que avanzamos de izquierda a derecha y de abajo hacia arriba.
¿Cómo influye el tamaño del átomo en la densidad?
El tamaño del átomo puede influir en la densidad de un elemento. En general, a medida que aumenta el tamaño del átomo, disminuyen las fuerzas de atracción entre los átomos, lo que puede resultar en una menor densidad. Por otro lado, los átomos más pequeños tienden a estar más densamente empaquetados, lo que resulta en una mayor densidad.
¿Cuál es la relación entre la conductividad eléctrica y la estructura atómica en la tabla periódica?
Los metales tienen una alta conductividad eléctrica debido a su estructura metálica, que permite un fácil movimiento de los electrones en el material. Por otro lado, los no metales, que tienen una estructura más compacta, tienden a tener una baja conductividad eléctrica debido a la falta de electrones móviles.
* Este artículo ha sido escrito por un copywriter experto en escribir artículos SEO en HTML en base al tema proporcionado. No se ha copiado ni pegado contenido de otras fuentes.