En el fascinante mundo de la química, entender las propiedades atómicas y su variación periódica es fundamental. La estructura de los átomos, sus componentes y su comportamiento pueden resultar confusos para algunos, pero son esenciales para comprender y explicar una amplia gama de fenómenos químicos. En esta guía completa, exploraremos cómo se organizan los átomos, cómo varían sus propiedades en la tabla periódica y cómo esto afecta las interacciones químicas.
¿Qué es un átomo y cómo se organiza?
Un átomo es la unidad básica de la materia. Está compuesto por un núcleo central que contiene protones y neutrones, rodeado por electrones que orbitan alrededor del núcleo en niveles de energía. Cada uno de estos componentes juega un papel crucial en las propiedades del átomo.
En el núcleo, los protones tienen carga positiva y los neutrones son neutros. Los electrones, por otro lado, tienen carga negativa y están distribuidos en diferentes niveles de energía, o capas electrónicas, alrededor del núcleo. Estas capas electrónicas se denominan K, L, M, N, O, P, Q, siendo K la más cercana al núcleo.
Propiedades atómicas y su variación periódica
Cada átomo tiene características únicas que están determinadas por el número de protones, neutrones y electrones que posee. Esto se refleja en las propiedades atómicas como el tamaño, la electronegatividad, la energía de ionización, la afinidad electrónica y la actividad química.
La variación periódica de las propiedades atómicas se refiere a cómo estas propiedades cambian de manera predecible a medida que se mueve a lo largo de la tabla periódica. La tabla periódica es una herramienta poderosa que muestra la organización de los elementos químicos en función de su número atómico.
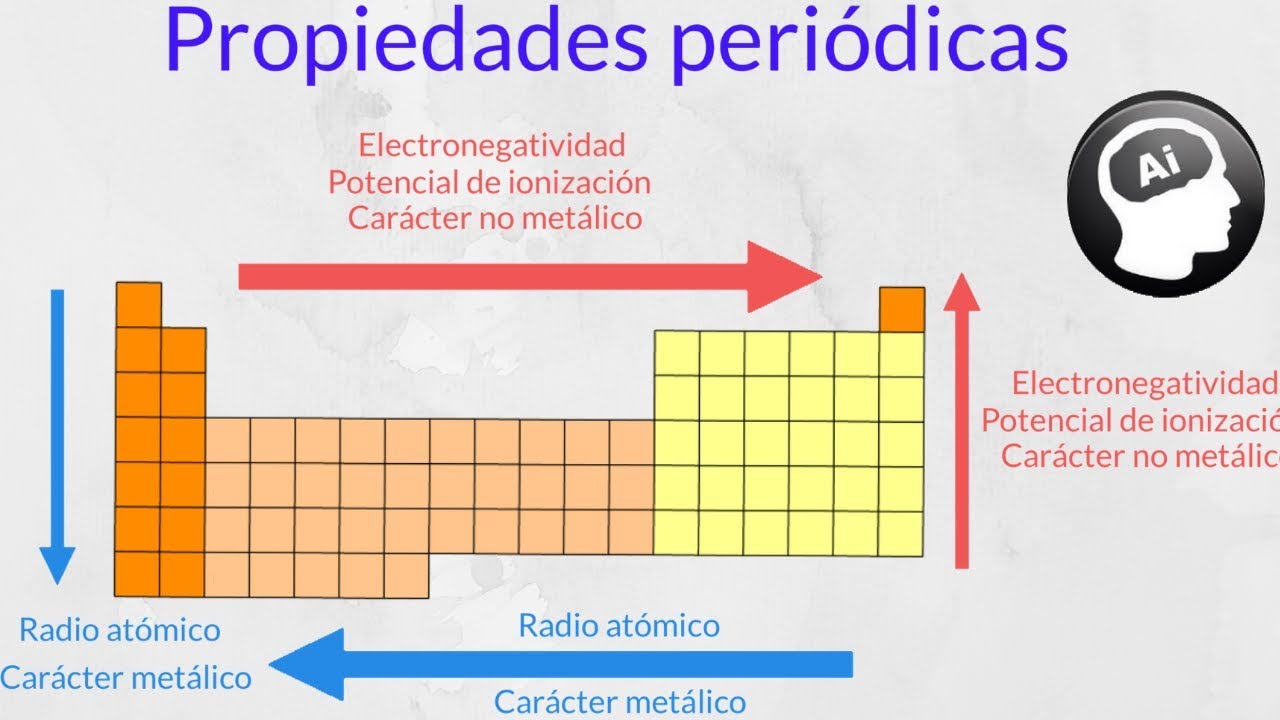
Tabla periódica y su relación con las propiedades atómicas
La tabla periódica está compuesta por filas horizontales llamadas periodos y columnas verticales llamadas grupos o familias. A medida que se avanza en un periodo de la tabla periódica de izquierda a derecha, el tamaño de los átomos disminuye. Esto se debe a que hay una mayor carga nuclear efectiva, lo que atrae a los electrones de las capas exteriores hacia el núcleo.
En cuanto a los grupos, los elementos que pertenecen al mismo grupo tienen configuraciones electrónicas similares y, por lo tanto, exhiben propiedades químicas similares. Elementos como el sodio y el potasio, por ejemplo, pertenecen al grupo 1 (también conocido como los metales alcalinos) y comparten características como su reactividad y capacidad para formar compuestos iónicos.
La relación entre las propiedades atómicas y las reacciones químicas
La comprensión de las propiedades atómicas y su variación periódica es esencial para entender las reacciones químicas. Las reacciones químicas ocurren cuando los átomos se unen, se separan o se intercambian electrones para formar nuevas sustancias.
La electronegatividad, por ejemplo, es una propiedad atómica que determina la capacidad de un átomo para atraer electrones en una reacción química. Los elementos con alta electronegatividad tienden a atraer electrones con mayor facilidad, lo que los hace más propensos a formar enlaces iónicos o covalentes con otros elementos.
En cambio, la energía de ionización es la cantidad de energía necesaria para quitar un electrón de un átomo neutro. Los elementos con alta energía de ionización tienen una gran tendencia a no perder electrones y, por lo tanto, son menos reactivos. Por otro lado, los elementos con baja energía de ionización tienden a perder electrones con facilidad, lo que los hace más propensos a formar cationes positivos.
Aplicaciones de las propiedades atómicas en la vida cotidiana
Las propiedades atómicas y su variación periódica no solo son importantes en un entorno científico, sino que también son relevantes en la vida cotidiana. Por ejemplo, el conocimiento de la electronegatividad y las propiedades de los enlaces químicos es fundamental en la industria de los materiales y la fabricación de productos.
La capacidad de comprender y predecir cómo los átomos interactúan entre sí ha permitido desarrollar materiales innovadores, como aleaciones metálicas más resistentes y ligeros, plásticos más duraderos y fibras textiles más resistentes. Además, las propiedades atómicas también juegan un papel importante en la medicina, la agricultura y la ciencia ambiental, entre otros campos.
¿Cuál es la diferencia entre el número atómico y la masa atómica?
El número atómico de un átomo es la cantidad de protones en su núcleo, mientras que la masa atómica es la suma de los protones y los neutrones. La masa atómica se expresa generalmente en unidades de masa atómica unificada (uma) o dalton (Da).
¿Qué es la electronegatividad y cómo afecta a los enlaces químicos?
La electronegatividad es la capacidad de un átomo para atraer electrones en un enlace químico. Los átomos con mayor electronegatividad tienden a atraer electrones con mayor fuerza, lo que lleva a la formación de enlaces covalentes polarizados o iónicos.
¿Cuál es la relación entre los grupos de la tabla periódica y las propiedades atómicas?
Los elementos que pertenecen al mismo grupo tienen configuraciones electrónicas similares, lo que implica que también comparten propiedades químicas similares. Por ejemplo, los elementos del grupo 1 (los metales alcalinos) tienen una tendencia a formar cationes y ser altamente reactivos.
Explorar las propiedades atómicas y su variación periódica es una ventana fascinante hacia el mundo de la química. Desde la estructura de los átomos hasta la forma en que interactúan y reaccionan, estas propiedades son fundamentales para comprender la ciencia detrás de la materia. ¡Sigue explorando y descubriendo cómo los átomos y sus propiedades afectan el mundo que nos rodea!