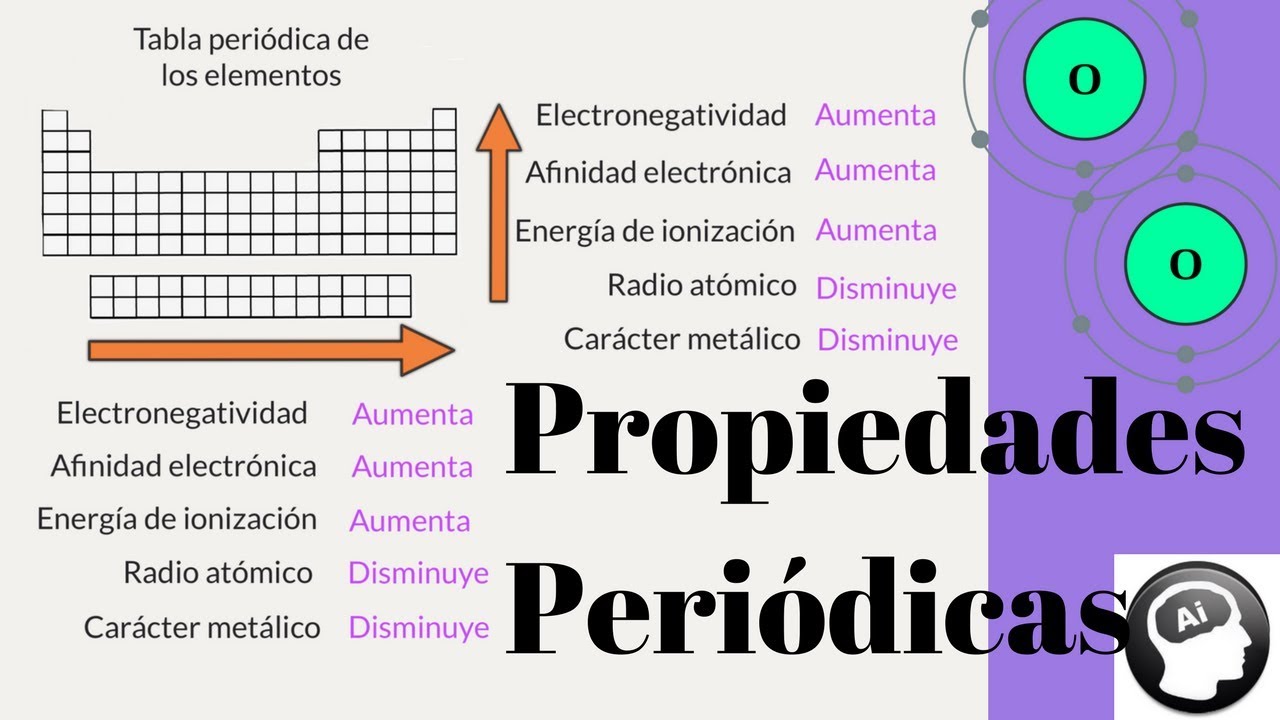
La química es una ciencia fascinante que estudia la composición, estructura, propiedades y transformaciones de la materia. Uno de los aspectos más interesantes de la química es la variación periódica de las propiedades químicas de los elementos. A lo largo de la tabla periódica, podemos observar patrones en las propiedades de los elementos, lo que nos permite predecir su comportamiento y entender mejor cómo se relacionan entre sí. En este artículo, exploraremos en detalle esta fascinante variación periódica y su importancia en la química.
¿Qué es la variación periódica de las propiedades químicas?
La variación periódica de las propiedades químicas se refiere a los patrones observados en las propiedades de los elementos a medida que aumenta su número atómico. Estos patrones se deben a la estructura electrónica de los átomos y cómo esta influye en sus características químicas. Los científicos han agrupado los elementos con propiedades similares en columnas llamadas grupos o familias en la tabla periódica, lo que facilita el estudio y la comprensión de estas tendencias periódicas.
Los períodos y las filas en la tabla periódica
La tabla periódica se organiza en períodos y filas. Los períodos representan las filas horizontales de la tabla, y cada período corresponde a un nivel energético o capa electrónica en un átomo. Por ejemplo, el primer período contiene solo dos elementos, hidrógeno y helio, que tienen una única capa electrónica. A medida que avanzamos en los períodos, encontramos más elementos con capas electrónicas adicionales.
Las filas, por otro lado, representan las columnas verticales de la tabla, y cada fila tiene elementos con características químicas similares. Por ejemplo, la primera fila o el primer período contiene los elementos alcalinos, que son altamente reactivos, mientras que la segunda fila o el segundo período contiene los elementos alcalinotérreos, que también tienen cierta reactividad pero en menor grado.
Tendencias periódicas en tamaño atómico
Una de las principales tendencias periódicas observadas en la tabla periódica es el tamaño atómico, es decir, el tamaño de los átomos de un elemento. En general, a medida que nos desplazamos hacia abajo en un grupo, los átomos tienden a volverse más grandes. Esto se debe a que los electrones están ocupando un nivel energético más alto y, por lo tanto, se encuentran más alejados del núcleo.
Por otro lado, a medida que nos desplazamos de izquierda a derecha en un período, los átomos tienden a volverse más pequeños. Esto se debe a que el número de protones en el núcleo aumenta, lo que atrae a los electrones más fuertemente hacia el núcleo y hace que el átomo sea más compacto.
Tendencias periódicas en electronegatividad
Otra tendencia periódica importante es la electronegatividad, que mide la capacidad de un átomo para atraer electrones hacia sí mismo en un enlace químico. En general, a medida que nos desplazamos hacia arriba en un grupo, la electronegatividad disminuye. Esto se debe a que los electrones están más alejados del núcleo y, por lo tanto, son menos atraídos por él.
Por otro lado, a medida que nos desplazamos de izquierda a derecha en un período, la electronegatividad tiende a aumentar. Esto se debe a que el número de protones en el núcleo aumenta, lo que aumenta la atracción que el átomo ejerce sobre los electrones.
Otras tendencias periódicas
Además del tamaño atómico y la electronegatividad, existen otras tendencias periódicas en las propiedades químicas de los elementos. Algunas de estas incluyen la energía de ionización (energía requerida para eliminar un electrón de un átomo), la afinidad electrónica (energía liberada cuando un átomo gana un electrón) y la reactividad química en general.
Estas tendencias periódicas nos ayudan a comprender mejor cómo los elementos interactúan entre sí y cómo se forman los enlaces químicos. También nos permiten predecir propiedades y comportamientos de elementos que aún no han sido estudiados en detalle.
Importancia de la variación periódica en la química
La variación periódica de las propiedades químicas es fundamental en el estudio de la química porque nos proporciona una base para entender cómo los elementos se relacionan entre sí y cómo se comportan en diferentes situaciones químicas. Al comprender estas tendencias, podemos predecir las propiedades de elementos desconocidos y diseñar compuestos con características específicas.
Por ejemplo, la variación periódica nos ayuda a entender por qué el sodio es altamente reactivo y forma compuestos iónicos con cloro para formar la sal de mesa, mientras que el neón es un gas inerte que no reacciona fácilmente con otros elementos. Esta comprensión de las tendencias periódicas también ha llevado al desarrollo de la química computacional, que utiliza modelos matemáticos y simulaciones para predecir y analizar propiedades químicas.
Además, la variación periódica tiene aplicaciones prácticas en diversos campos, como la medicina, la agricultura y la industria. Por ejemplo, la variación periódica se utiliza para determinar dosis de medicamentos, diseñar fertilizantes y seleccionar materiales adecuados para construir dispositivos electrónicos.
En conclusión, la variación periódica de las propiedades químicas es un fenómeno fascinante que nos permite entender mejor cómo los elementos se comportan y se relacionan entre sí. Las tendencias periódicas en tamaño atómico, electronegatividad y otras propiedades químicas son fundamentales en el estudio y la aplicación de la química. Al comprender estas tendencias, podemos predecir propiedades, diseñar compuestos y mejorar nuestra comprensión del mundo que nos rodea.
1. ¿Cuál es la importancia de la variación periódica en la química?
La variación periódica es importante en la química porque nos permite predecir las propiedades de elementos desconocidos, entender cómo se relacionan los elementos entre sí y diseñar compuestos con características específicas.
2. ¿Qué es la electronegatividad?
La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo en un enlace químico. Cuanto mayor sea la electronegatividad, mayor será la atracción que el átomo ejerce sobre los electrones.
3. ¿Cómo varía el tamaño atómico a lo largo de la tabla periódica?
En general, los átomos tienden a volverse más grandes a medida que nos desplazamos hacia abajo en un grupo y más pequeños a medida que nos desplazamos de izquierda a derecha en un período.
4. ¿Qué otras propiedades químicas varían periódicamente?
Además del tamaño atómico y la electronegatividad, propiedades como la energía de ionización, la afinidad electrónica y la reactividad química general también varían periódicamente a lo largo de la tabla periódica.