¿Qué es la estructura atómica de la materia?
La estructura atómica de la materia es el estudio de la composición básica de todas las cosas que nos rodean. Los átomos son las unidades fundamentales de la materia y están compuestos por protones, neutrones y electrones. Estas partículas se unen de diversas formas para formar moléculas y compuestos, lo que determina las propiedades y comportamientos de los objetos que vemos en nuestro día a día.
La importancia de comprender la estructura atómica
Para comprender cómo funcionan las cosas a nivel más profundo, es crucial entender la estructura atómica de la materia. Esta comprensión nos permite explicar fenómenos y procesos químicos, así como entender las propiedades de los materiales y cómo interactúan entre sí.
Entender la estructura atómica es fundamental en campos como la ciencia de materiales, la química y la física. Además, también tiene aplicaciones prácticas en industrias como la medicina, la ingeniería y la tecnología.
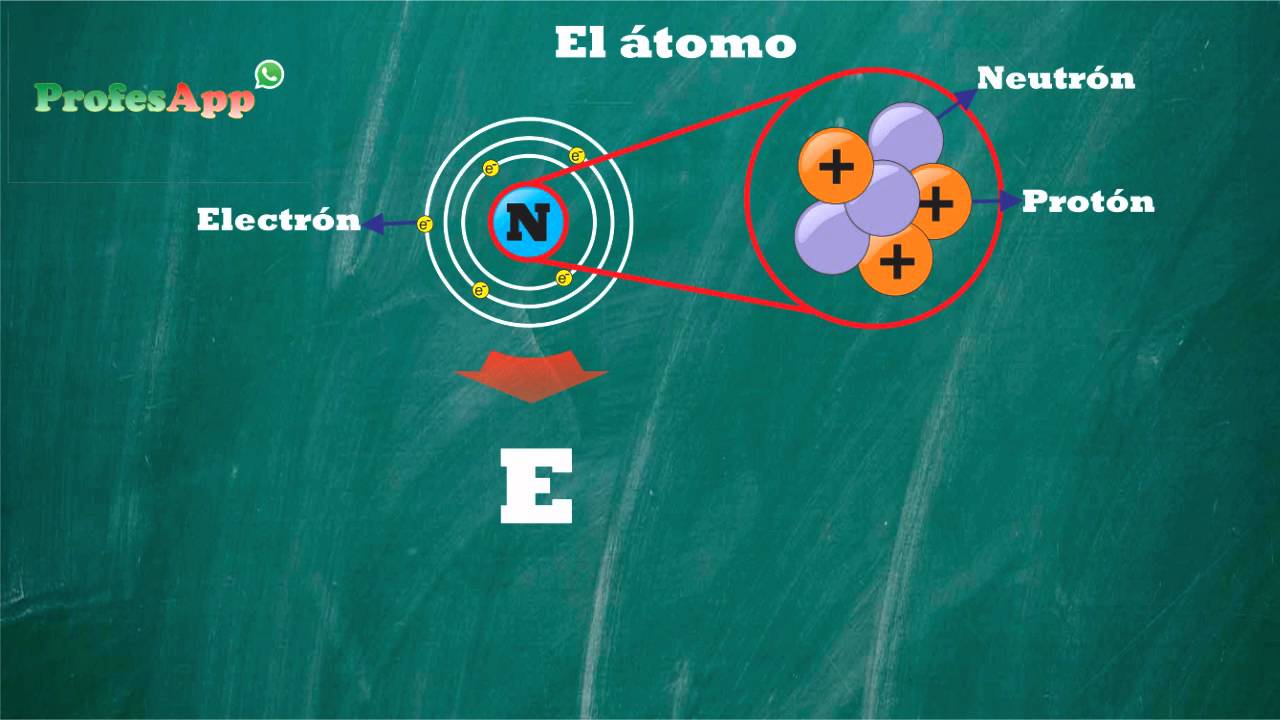
La estructura básica del átomo
Un átomo se compone de un núcleo central, donde se encuentran los protones y neutrones, y una nube de electrones que orbitan alrededor del núcleo. Los protones tienen carga eléctrica positiva, mientras que los electrones tienen carga negativa. Los neutrones, por su parte, no tienen carga. La cantidad de protones en el núcleo determina el número atómico del átomo, mientras que la suma de protones y neutrones determina su masa atómica.
¿Qué son los electrones?
Los electrones son partículas subatómicas que orbitan alrededor del núcleo del átomo. Tienen carga eléctrica negativa y son mucho menos masivos que los protones y neutrones. Los electrones se distribuyen en diferentes niveles de energía llamados capas o niveles de electrones. Cada nivel tiene un límite en la cantidad de electrones que puede alojar, y los electrones tienden a llenar primero los niveles de menor energía antes de pasar a niveles de mayor energía.
¿Qué son los protones?
Los protones son partículas subatómicas que se encuentran en el núcleo del átomo. Tienen carga eléctrica positiva y tienen una masa similar a la de los neutrones. Los protones se unen por la fuerza nuclear fuerte, que es una de las fuerzas fundamentales de la naturaleza. El número de protones en el núcleo de un átomo determina su identidad y su número atómico.
¿Qué son los neutrones?
Los neutrones son partículas subatómicas que también se encuentran en el núcleo del átomo. A diferencia de los protones y electrones, los neutrones no tienen carga eléctrica, lo que los hace eléctricamente neutros. Su masa es similar a la de los protones y también se unen por la fuerza nuclear fuerte. Los neutrones proporcionan estabilidad al núcleo atómico al contrarrestar las repulsiones de las cargas positivas de los protones.
La tabla periódica de los elementos
La tabla periódica de los elementos es una herramienta fundamental en el estudio de la estructura atómica de la materia. En la tabla, los elementos se organizan en filas y columnas según su número atómico y propiedades químicas. Cada elemento tiene una configuración electrónica única que determina su comportamiento químico.
Las filas de la tabla se denominan periodos, mientras que las columnas se conocen como grupos. Los elementos que se encuentran en la misma columna comparten características químicas similares debido a la configuración electrónica de sus átomos. La tabla periódica es una herramienta esencial para predecir cómo los átomos se unirán y reaccionarán entre sí.
Enlace químico y estructuras moleculares
Cuando los átomos se unen, forman moléculas y compuestos a través de enlaces químicos. Dependiendo de cómo se compartan, ganen o pierdan electrones, los átomos pueden formar enlaces covalentes, iónicos o metálicos.
Enlaces covalentes
Los enlaces covalentes se forman cuando dos átomos comparten electrones en su capa de valencia. Esto ocurre cuando ambos átomos necesitan electrones adicionales para completar su capa externa. Los enlaces covalentes pueden ser simples, múltiples o coordinados, dependiendo de la cantidad de electrones compartidos.
Enlaces iónicos
Los enlaces iónicos se forman cuando átomos con electronegatividades diferentes transfieren electrones. Un átomo dona uno o más electrones para formar iones positivos llamados cationes, mientras que otro átomo acepta esos electrones para formar iones negativos llamados aniones. Los cationes y aniones se atraen mutuamente debido a sus cargas opuestas, lo que crea un enlace iónico.
Enlaces metálicos
Los enlaces metálicos ocurren en metales, donde los electrones están débilmente ligados a los átomos y se mueven libremente. Esto permite que los metales conductoras eléctricas y térmicas. Los electrones libres, también conocidos como electrones deslocalizados, se mueven a lo largo de la red metálica y se mantienen unidos por las fuerzas de atracción electromagnética.
Aplicaciones y conclusiones
Conocer la estructura atómica de la materia tiene numerosas aplicaciones en la ciencia y la tecnología. Desde el diseño de nuevos materiales y medicamentos hasta la comprensión de los procesos nucleares en estrellas y reactores nucleares, el estudio de la estructura atómica es esencial para avanzar en nuestra comprensión del mundo que nos rodea.
En conclusión, la fascinante estructura atómica de la materia nos permite entender cómo se componen y cómo interactúan los átomos. A través de la tabla periódica y el estudio de los enlaces químicos, podemos comprender las propiedades y comportamientos de la materia. Esta comprensión tiene aplicaciones prácticas en una amplia gama de campos y es fundamental para nuestro avance científico y tecnológico. ¿Quieres aprender más sobre la estructura atómica? ¡Sigue explorando y descubriendo las maravillas de la ciencia!