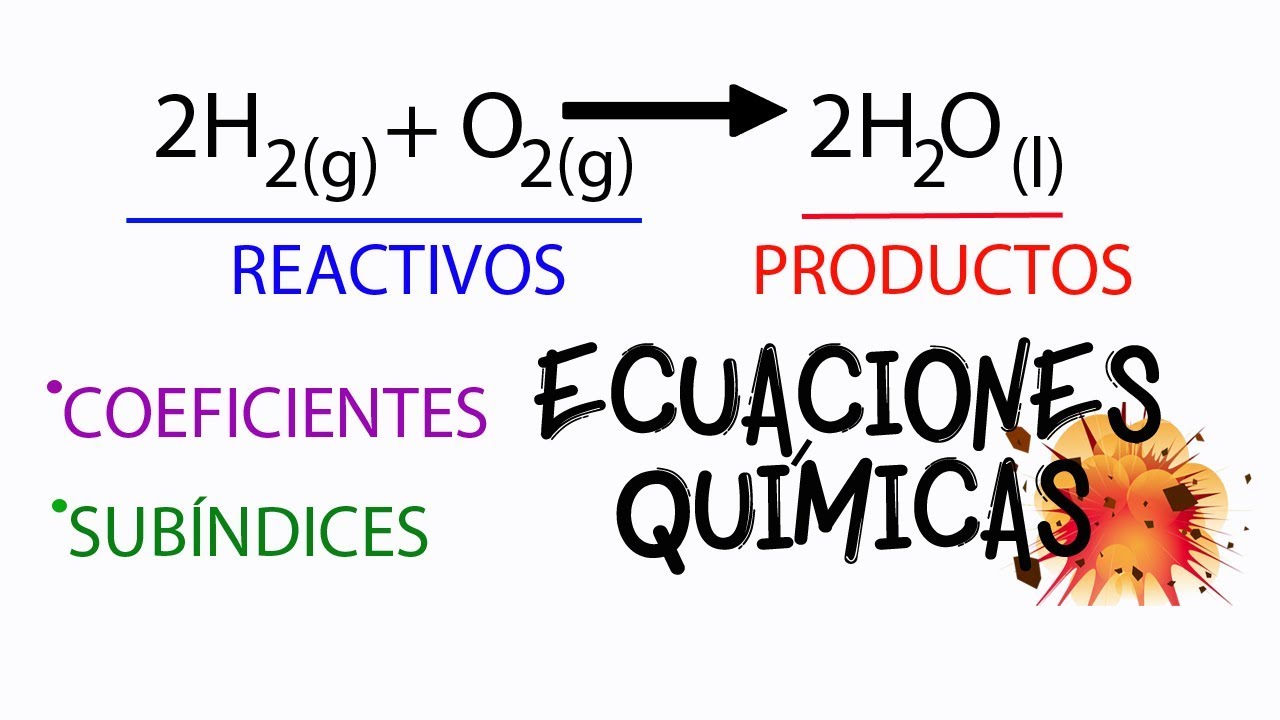
Como copywriter experto en escribir artículos SEO en HTML, me complace presentarte una guía completa con ejemplos sobre cómo identificar los reactivos en diferentes tipos de reacciones químicas. En este artículo, exploraremos los conceptos básicos de las reacciones químicas y aprenderemos cómo identificar los reactivos clave en algunas reacciones comunes. ¡Empecemos!
¿Qué son los reactivos en una reacción química?
Antes de sumergirnos en los ejemplos específicos de reacciones y sus reactivos, es importante comprender qué son los reactivos en una reacción química. En términos simples, los reactivos son las sustancias que interactúan entre sí para formar nuevos productos durante una reacción química. Estas sustancias pueden ser elementos o compuestos y son esenciales para que ocurra una reacción química.
Hidróxido de sodio y ácido clorhídrico
Uno de los ejemplos más comunes de una reacción química es la neutralización del ácido clorhídrico con hidróxido de sodio para formar cloruro de sodio y agua. En esta reacción, el ácido clorhídrico y el hidróxido de sodio son los reactivos clave.
El ácido clorhídrico (HCl) es un compuesto químico fuertemente ácido que se encuentra comúnmente en el estómago humano y se utiliza en diversos procesos industriales. Por otro lado, el hidróxido de sodio (NaOH), también conocido como sosa cáustica, es una base fuerte ampliamente utilizada en la fabricación de productos químicos y en la industria de alimentos y bebidas.
La reacción química entre el ácido clorhídrico y el hidróxido de sodio se produce de la siguiente manera:
HCl + NaOH → NaCl + H2O
En esta ecuación, el ácido clorhídrico y el hidróxido de sodio reaccionan entre sí para formar cloruro de sodio (NaCl) y agua (H2O). Los reactivos en esta reacción son el ácido clorhídrico y el hidróxido de sodio, mientras que los productos son el cloruro de sodio y el agua.
Óxido de zinc y ácido sulfúrico
Otro ejemplo interesante de una reacción química es la reacción entre el óxido de zinc y el ácido sulfúrico para formar sulfato de zinc y agua. En esta reacción, el óxido de zinc y el ácido sulfúrico son los reactivos fundamentales.
El óxido de zinc (ZnO) es un compuesto químico blanco y sólido que se utiliza en una variedad de aplicaciones industriales, como el recubrimiento de galvanizado y la fabricación de productos de caucho. El ácido sulfúrico (H2SO4), por otro lado, es un ácido fuerte que se encuentra comúnmente en la industria química y se utiliza en la producción de fertilizantes y productos químicos.
La reacción química entre el óxido de zinc y el ácido sulfúrico se representa de la siguiente manera:
ZnO + H2SO4 → ZnSO4 + H2O
En esta ecuación, el óxido de zinc y el ácido sulfúrico reaccionan entre sí para formar sulfato de zinc (ZnSO4) y agua (H2O). Recuerda que los reactivos son el óxido de zinc y el ácido sulfúrico, mientras que los productos son el sulfato de zinc y el agua.
Nitrito de sodio y ácido clorhídrico
Continuemos con nuestro próximo ejemplo de reacción química, que involucra el nitrito de sodio y el ácido clorhídrico. En esta reacción, el nitrito de sodio y el ácido clorhídrico son los reactivos principales.
El nitrito de sodio (NaNO2) es una sal inorgánica comúnmente utilizada en la conservación y curado de alimentos y como aditivo en productos cárnicos. Por otro lado, el ácido clorhídrico (HCl) ya lo hemos mencionado en nuestro primer ejemplo de neutralización.
La reacción química entre el nitrito de sodio y el ácido clorhídrico se puede representar de la siguiente manera:
NaNO2 + HCl → NaCl + HNO2
En esta ecuación, el nitrito de sodio y el ácido clorhídrico reaccionan entre sí para formar cloruro de sodio (NaCl) y ácido nitroso (HNO2). En este caso, los reactivos son el nitrito de sodio y el ácido clorhídrico, mientras que los productos son el cloruro de sodio y el ácido nitroso.
En resumen, los reactivos son las sustancias que interactúan entre sí para formar nuevos productos durante una reacción química. En los ejemplos anteriores, vimos tres reacciones diferentes y sus reactivos. Desde la neutralización del ácido clorhídrico con hidróxido de sodio hasta la reacción entre el óxido de zinc y el ácido sulfúrico, estos ejemplos ilustran cómo identificar los reactivos clave en diferentes tipos de reacciones químicas.
Espero que esta guía completa con ejemplos te haya resultado útil para comprender mejor los reactivos en las reacciones químicas. Si tienes alguna pregunta adicional o quieres aprender más sobre este tema, no dudes en dejar un comentario a continuación. ¡Nos encantaría ayudarte!
¿Cuál es la diferencia entre reactivos y productos en una reacción química?
Los reactivos son las sustancias que interactúan entre sí para formar nuevos productos durante una reacción química. Por otro lado, los productos son las sustancias que se forman como resultado de la reacción química. En resumen, los reactivos son los ingredientes y los productos son el resultado final de una reacción química.
¿Qué sucede si un reactivo falta en una reacción química?
Si un reactivo falta en una reacción química, la reacción no podrá completarse correctamente y los productos deseados no se formarán. Los reactivos son esenciales para que ocurra una reacción química, por lo que su ausencia o falta puede detener o alterar el proceso de reacción.
¿Cómo puedo identificar los reactivos en una reacción química?
Para identificar los reactivos en una reacción química, debes revisar la ecuación química que representa la reacción. Los reactivos se encuentran en el lado izquierdo de la flecha (→) en la ecuación, antes de los productos. Por lo general, se representan por las sustancias químicas que están interactuando entre sí en la reacción.
¿Cuál es la importancia de identificar los reactivos en una reacción química?
Identificar los reactivos en una reacción química es crucial para comprender y analizar el proceso de reacción. Esto nos permite entender cómo interactúan las sustancias químicas entre sí y qué productos se formarán como resultado. Además, identificar los reactivos es fundamental para realizar cálculos estequiométricos y determinar la cantidad de productos que se obtendrán en una reacción química.
¿Los reactivos siempre se consumen por completo en una reacción química?
En la mayoría de las reacciones químicas, los reactivos se consumen por completo para formar los productos. Sin embargo, en algunas reacciones, puede haber un exceso de un reactivo que no se consume por completo y se obtiene como exceso en los productos finales. Estas situaciones dependen de la estequiometría de la reacción y la proporción entre los reactivos.