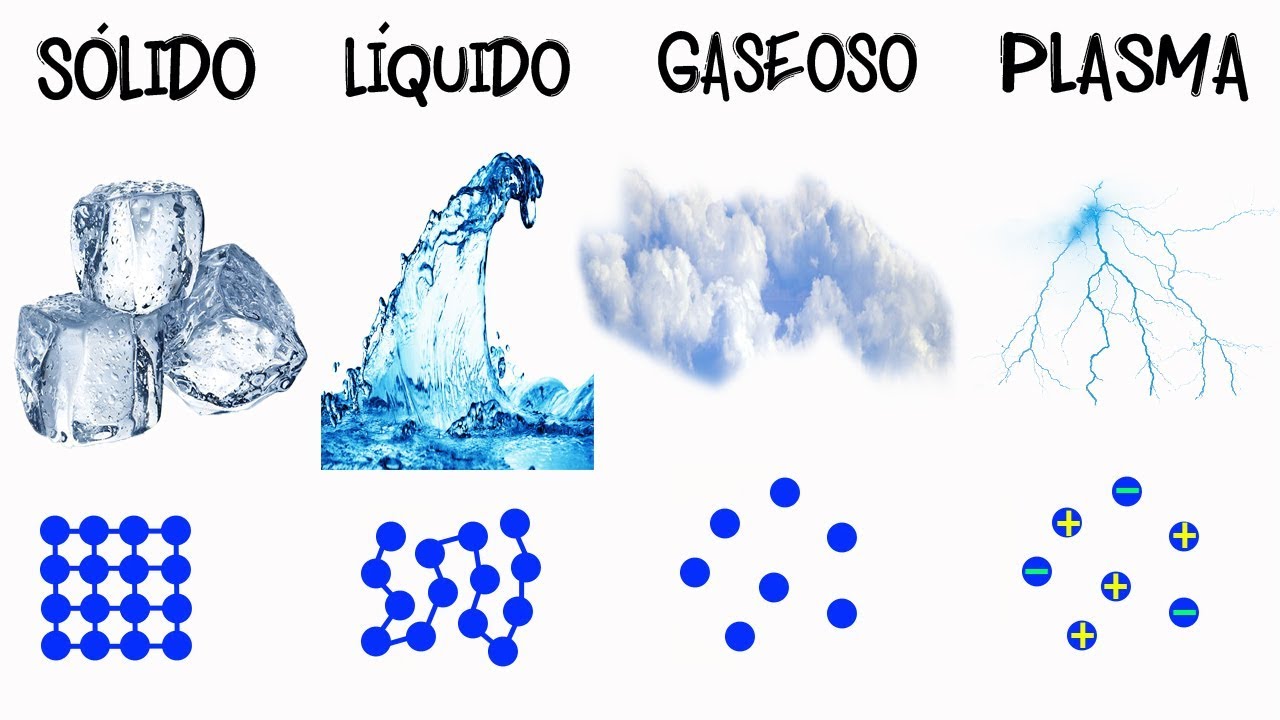
¿Qué son los estados de agregación?
Los estados de agregación, también conocidos como fases de la materia, son las formas en las que la materia se presenta en la naturaleza. Estos estados se caracterizan por la forma en que las partículas que componen la materia se organizan y se mueven entre sí. Los tres estados de agregación más comunes son el sólido, el líquido y el gaseoso. Cada uno de estos estados presenta propiedades físicas y comportamientos distintos.
Estado sólido
El estado sólido es aquel en el que las partículas que componen la materia están muy juntas y tienen una estructura ordenada. Esto significa que las partículas se mantienen en una posición fija y solo pueden vibrar alrededor de su posición de equilibrio. Los sólidos tienen una forma definida y un volumen constante, lo que significa que no se deforman fácilmente y ocupan un espacio específico.
Un ejemplo común de un sólido es el hielo. Las moléculas de agua se juntan en una estructura ordenada formando una red cristalina, lo que le otorga al hielo su forma rígida y su volumen constante.
Estado líquido
El estado líquido se caracteriza por tener partículas que están más separadas que en el estado sólido, lo que les permite moverse más libremente. En un líquido, las partículas mantienen una cercanía relativa pero no tienen una estructura ordenada como en los sólidos. Esto significa que las partículas pueden moverse y fluir entre sí.
Los líquidos toman la forma del recipiente que los contiene y ocupan un volumen específico. Ejemplos comunes de líquidos son el agua, el aceite y el jugo. Estos líquidos pueden fluir, cambiar de forma y ocupar diferentes volúmenes según el recipiente en el que se encuentren.
Estado gaseoso
El estado gaseoso es aquel en el que las partículas se encuentran separadas y se mueven libremente en todas las direcciones. En este estado, las partículas tienen una energía cinética alta y están muy distantes unas de otras. No tienen una estructura ordenada y ocupan todo el espacio disponible.
El gas se expande para llenar el recipiente en el que se encuentra y no tiene una forma ni un volumen definido. Ejemplos de gases son el oxígeno, el nitrógeno y el dióxido de carbono. Estos gases pueden llenar un espacio completamente y se mezclan fácilmente entre sí.
¿Cómo ocurren los cambios de estado?
Los cambios de estado ocurren cuando una sustancia pasa de un estado de agregación a otro debido a cambios en la temperatura y/o presión. Estos cambios se pueden clasificar en dos categorías principales: cambios de fase endotérmicos y exotérmicos.
Cambios de fase endotérmicos
Los cambios de fase endotérmicos ocurren cuando una sustancia absorbe energía del entorno y la temperatura de la sustancia aumenta. En estos casos, las partículas ganan energía y la movilidad aumenta, lo que resulta en un cambio de estado. Ejemplos de cambios de fase endotérmicos son la fusión y la vaporización.
– Fusión: La fusión es el cambio de estado de un sólido a un líquido debido a un aumento en la temperatura. Durante la fusión, las partículas del sólido obtienen suficiente energía térmica para vencer las fuerzas de atracción entre ellas y empiezan a moverse más libremente.
– Vaporización: La vaporización es el cambio de estado de un líquido a un gas debido a una adición de energía térmica. Durante la vaporización, las partículas del líquido ganan energía suficiente para romper las fuerzas de cohesión y pasar al estado gaseoso.
Cambios de fase exotérmicos
Los cambios de fase exotérmicos ocurren cuando una sustancia libera energía al entorno y la temperatura de la sustancia disminuye. En estos casos, las partículas pierden energía y disminuye su movilidad, lo que resulta en un cambio de estado. Ejemplos de cambios de fase exotérmicos son la solidificación y la condensación.
– Solidificación: La solidificación es el cambio de estado de un líquido a un sólido debido a una disminución en la temperatura. Durante la solidificación, las partículas del líquido pierden energía térmica y se agrupan en una estructura ordenada, formando un sólido.
– Condensación: La condensación es el cambio de estado de un gas a un líquido debido a una disminución en la temperatura. Durante la condensación, las partículas del gas pierden energía térmica y se agrupan formando un líquido.
¿Cuál es el cuarto estado de agregación?
Además de los estados sólido, líquido y gaseoso, existe un cuarto estado de agregación llamado plasma. El plasma se encuentra en condiciones extremadamente calientes y consiste en una mezcla de partículas cargadas, como electrones y iones. El plasma se encuentra en lugares como el sol y las estrellas, así como en dispositivos como los televisores de plasma.
¿Puede una sustancia cambiar directamente de un estado de agregación a otro?
Sí, en ciertos casos una sustancia puede cambiar directamente de un estado de agregación a otro sin pasar por el estado intermedio. Este proceso se conoce como sublimación (cambio de sólido a gas) y deposición (cambio de gas a sólido). Ejemplos comunes de sustancias que subliman son el hielo seco (dióxido de carbono sólido) y el alcanfor.
¿Por qué algunas sustancias pueden existir en diferentes estados de agregación a diferentes temperaturas?
La existencia de diferentes estados de agregación de una sustancia a diferentes temperaturas se debe a las fuerzas de atracción y repulsión entre las partículas que componen la sustancia. Estas fuerzas dependen de la energía cinética de las partículas, que a su vez está relacionada con la temperatura. A temperaturas altas, las partículas tienen suficiente energía para vencer las fuerzas de atracción y pasar al estado gaseoso, mientras que a temperaturas más bajas, estas fuerzas son más fuertes y mantienen las partículas más juntas en estados sólidos o líquidos.
¿Cómo afecta la presión a los estados de agregación?
La presión también puede afectar los estados de agregación de una sustancia. En general, un aumento en la presión tiende a favorecer la formación de estados más densos, como los líquidos o los sólidos. Por otro lado, una disminución en la presión puede favorecer la formación de estados más dispersos, como los gases. Sin embargo, es importante tener en cuenta que la influencia de la presión en los cambios de estado depende de la sustancia y de las condiciones específicas en las que se encuentre.
¡Ahora que has descubierto el esquema de los estados de agregación paso a paso, estás listo para comprender mejor las diferentes formas en que la materia puede existir en la naturaleza! Si tienes alguna pregunta adicional sobre este tema, no dudes en dejarla en los comentarios. Estaré encantado de ayudarte a aclarar cualquier duda que puedas tener.